파키스탄은 로슈의 항암제 아바스틴(Avastin)을 주사한 당뇨병 환자 12명이 시력을 잃은 후, 이 약의 유통업체 두 곳을 조사하고 있습니다. 아바스틴은 베트남에서도 허가를 받았습니다.
베트남에서는 9월 27일 현재, 베트남 의약품 관리국( 보건부 )은 아바스틴을 사용한 후 시력을 잃은 환자와 관련된 아바스틴의 바람직하지 않은 효과를 반영하는 보고를 접수하지 않았습니다.
베트남 약품관리국은 F. Hoffmann La Roche Ltd. 대표 사무소로부터 해당 사건에 대한 보고서를 받았습니다.
특히 파키스탄에서는 불법 공급업체인 Genius Pharmaceutical Service에서 공급한 주사제를 사용한 환자 약 12명이 시력을 잃었습니다. 해당 약물에는 "주사제 아바스틴 1.25mg/0.05ml"라는 라벨이 붙어 있어 로슈 제품이라는 잘못된 인식을 심어주었습니다.
로슈의 아바스틴은 안과용으로 승인되지 않았습니다. Genius Pharmaceutical Service는 비위생적이고 승인되지 않은 환경에서 1.25mg/0.5ml 용량을 공급/희석/재포장했습니다.
파키스탄 당국은 오염 원인을 조사 중입니다. 불충분한 살균, 오염된 바이알, 살균되지 않은 주사기, 그리고 약물 조제 과정에서 표준 운영 절차 위반 등이 원인으로 추정됩니다.
동시에 파키스탄 정부는 로슈의 아바스틴 100mg/ml(H352B11, B7266B07, B7266B20) 3개 배치와 Genius Pharmaceutical Service에서 공급한 모든 약물에 대한 리콜을 요청했습니다.
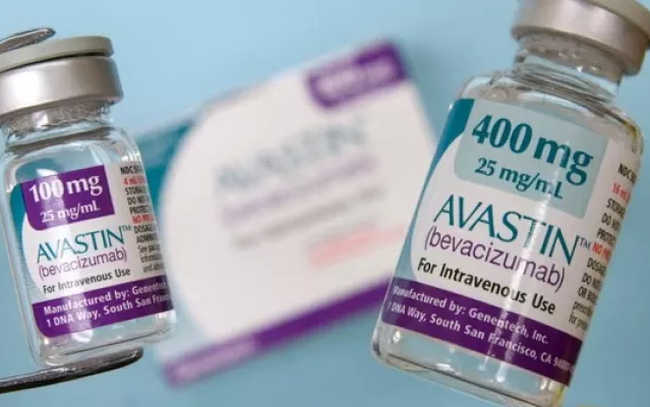
(그림: 24 뉴스 HD).
베트남에서는 아바스틴(활성 성분 베바시주맙)이 4건의 유통 등록증을 취득했으며, 모두 현재 유효합니다. 다음을 포함합니다.
베바시주맙 100mg/4ml(1 바이알 x 4ml 상자; 등록 번호: 400410250123(QLSP-1118-18); 제조업체: Roche Diagnostics GmbH, 독일).
베바시주맙 400mg/16ml(1 바이알 x 16ml 상자: 등록 번호: 400410250223(QLSP-1119-18); 제조업체: Roche Diagnostics GmbH, 독일).
베바시주맙 100mg/4ml(1 바이알 x 16ml 상자; 등록 번호: QLSP-1010-17; 제조업체: F. Hoffmann-La Roche Ltd., 스위스).
베바시주맙 400mg/16ml(1 바이알 x 16ml 상자; 등록 번호: QLSP-1011-17; 제조업체: F. Hoffmann-La Roche Ltd., 스위스).
아바스틴은 베트남에서 전이성 대장암, 진행성, 전이성 또는 재발성 비소세포 폐암, 진행성 및/또는 전이성 신세포 암, 신경교종/악성 신경교종(WHO 4기), 상피성 난소암, 나팔관암 및 원발성 복막암을 포함한 특정 암의 치료를 위해 허가를 받았습니다.
일반적인 경고 외에도 FDA 승인 패키지 삽입물에는 "유리체내 사용 금지"에 대한 경고가 포함되어 있습니다.
구체적으로, 이 약물은 시각 장애를 일으킬 수 있으며, 암 환자의 정맥 주입을 위한 바이알에 들어 있는 아바스틴 혼합물을 투여하는 승인되지 않은 투여 경로인 유리체내 주사 후 심각한 눈 부작용 사례와 군집이 보고되었습니다.
이러한 반응에는 안구 내 감염, 안내염, 포도막염, 망막 박리, 망막 색소 상피 파열, 녹내장, 안구 내 출혈 등이 포함됩니다. 이러한 사건 중 일부는 영구 실명을 포함한 다양한 정도의 시야 손실을 초래했습니다 .
[광고_2]
원천







































































































댓글 (0)