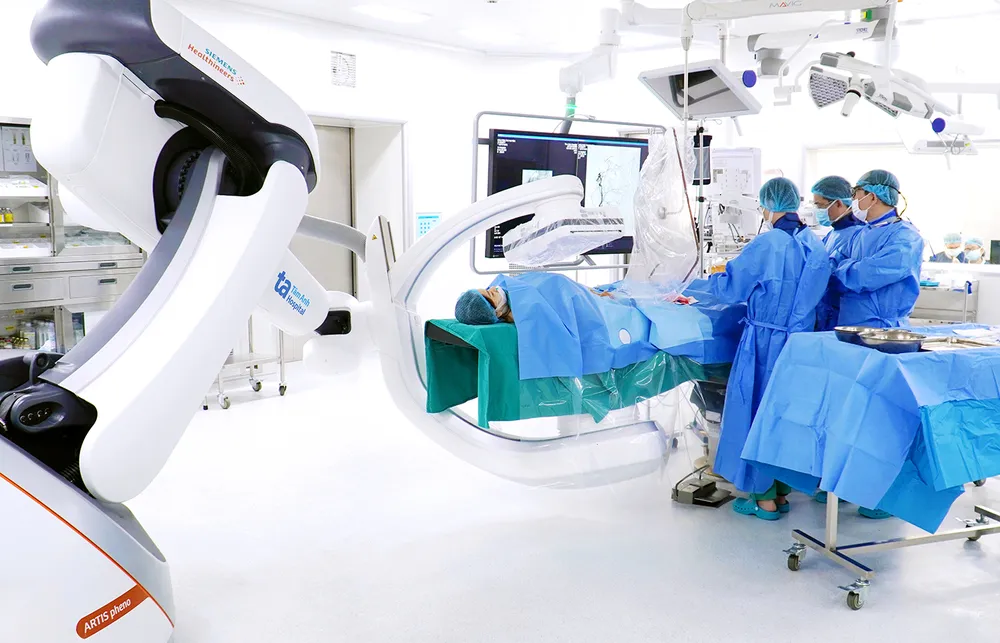
ลดต้นทุน เพิ่มโอกาสการรักษา
ปลายเดือนธันวาคม พ.ศ. 2567 สถาบันวิจัยทัมอันห์ได้ดำเนินโครงการ VISTA-1 เกี่ยวกับยาภูมิคุ้มกันบำบัดชนิดรับประทานสำหรับการรักษามะเร็งในเวียดนาม หลังจากการทดสอบเกือบ 6 เดือน ผู้ป่วยมะเร็งลำไส้ใหญ่ระยะลุกลามจำนวน 8 รายได้รับการรักษาตามระเบียบปฏิบัติการวิจัย โดยไม่มีผลข้างเคียงที่สำคัญจากยาที่ใช้ในการวิจัย และพบสัญญาณบวกในเบื้องต้น
ในฐานะบุคคลแรกที่ทดสอบยาในโครงการนี้ คุณเอ็ม (อายุ 50 ปี) ผู้ป่วยมะเร็งลำไส้ใหญ่และทวารหนักที่แพร่กระจายไปที่ตับ กล่าวว่าเขาได้รับการรักษาด้วยวิธีการต่างๆ เช่น เคมีบำบัดและยาที่ออกฤทธิ์เฉพาะที่ แต่ไม่ได้ตอบสนองต่อการรักษา ในเดือนมกราคม พ.ศ. 2568 เขาได้ลงทะเบียนเข้าร่วมการศึกษาและได้รับการประเมินว่ามีสิทธิ์เข้าร่วม “ผมเคยคิดว่าผมไม่มีทางเลือกอื่น แต่ด้วยโอกาสที่ได้เข้าร่วมการศึกษานี้ ผมรู้สึกโล่งใจและมีความหวังมากขึ้น” คุณเอ็ม กล่าว
ดร. หวู ฮู เคียม หัวหน้าแผนกมะเร็งวิทยา โรงพยาบาลทัม อันห์ กรุง ฮานอย กล่าวว่า ผู้ป่วยที่เข้าร่วมการศึกษาจะได้รับการติดตามอย่างใกล้ชิดเพื่อความปลอดภัยและการตอบสนองต่อยาวิจัย ทีมวิจัยไม่ได้บันทึกอาการผิดปกติใดๆ ที่เกี่ยวข้องกับยาวิจัยในผู้ป่วยที่ใช้ยานี้ในช่วง 3 เดือนที่ผ่านมา
“สำหรับผู้ป่วยมะเร็งลำไส้ใหญ่และทวารหนักระยะลุกลามที่ไม่ตอบสนองต่อการรักษาในปัจจุบัน การปรับปรุงระยะเวลาการรอดชีวิตในแต่ละขั้นตอนการวิจัยนั้นมีความหมายอย่างยิ่ง ขณะนี้เราและผู้ป่วยได้เข้าสู่เดือนที่สี่ของการดำเนินการวิจัยนี้แล้ว” ดร. หวู่ ฮู เคียม กล่าว
ณ โรงพยาบาลมะเร็งนครโฮจิมินห์ ดร. ฟาน ตัน ทวน หัวหน้าหน่วยทดลองทางคลินิก กล่าวว่า ขณะนี้หน่วยกำลังดำเนินการวิจัยทางคลินิก 37 โครงการ ซึ่งส่วนใหญ่ร่วมมือกับบริษัทยาข้ามชาติ (Pharma) ส่วนหนึ่งเป็นเพราะโรงพยาบาลยังประสานงานกับศูนย์มะเร็งในภูมิภาคอย่างแข็งขันเพื่อดำเนินการวิจัยอิสระที่มีคุณค่าทางวิชาการและการประยุกต์ใช้จริง โรงพยาบาลมักใช้ยารุ่นใหม่เพื่อเปรียบเทียบกับสูตรยามาตรฐานที่ใช้อยู่ในปัจจุบัน ยาเหล่านี้หลายชนิดยังไม่มีจำหน่ายในเวียดนามและมีราคาแพงมาก บางชนิดมีราคาสูงถึง 300 ล้านดองเวียดนามต่อรอบการรักษา (3-4 สัปดาห์) ผู้ป่วยที่เข้าร่วมโครงการจะได้รับยาฟรีไม่ว่าจะอยู่ในสาขาใดก็ตาม
นอกจากจะช่วยให้ผู้ป่วยเข้าถึงการรักษาสมัยใหม่ได้เร็วขึ้นแล้ว การศึกษาเหล่านี้ยังสร้างเงื่อนไขให้ผู้เชี่ยวชาญในประเทศสามารถรวบรวมข้อมูลและประเมินประสิทธิภาพของยาในประชากรเวียดนามได้ ซึ่งจะทำให้ระยะเวลาในการนำยาใหม่ๆ ออกสู่ตลาดสั้นลง ยารุ่นใหม่หลายตัวมีราคาแพงมาก ที่นี่เราให้ผู้ป่วยที่เข้าร่วมการศึกษาเข้าถึงยารุ่นใหม่ได้ฟรี เมื่อยาที่ใช้ในการวิจัยประสบความสำเร็จ ก็จะช่วยลดระยะเวลาในการนำยาใหม่ๆ ออกสู่ตลาดได้” ดร. ฟาน ตัน ทวน กล่าว
การทดลองทางคลินิกในช่วงที่ผ่านมาช่วยให้อุตสาหกรรม การแพทย์ เข้าถึงวิธีการรักษาสมัยใหม่ได้อย่างรวดเร็ว ตั้งแต่เคมีบำบัดแบบดั้งเดิม ไปจนถึงภูมิคุ้มกันบำบัด และยาที่ออกฤทธิ์เฉพาะจุด ความก้าวหน้าเหล่านี้ไม่เพียงแต่ช่วยยืดอายุผู้ป่วยเท่านั้น แต่ยังช่วยยกระดับคุณภาพชีวิตของผู้ป่วย ขณะเดียวกันก็ขยายการเข้าถึงยาใหม่ๆ ในต้นทุนที่ต่ำลงสำหรับผู้ป่วยและระบบการแพทย์อีกด้วย
รัฐมนตรีช่วย ว่าการกระทรวงสาธารณสุข เหงียนถิเหลียนเฮือง
มีศักยภาพมาก แต่ขาดกลไก
ศาสตราจารย์กาย ธเวทส์ ผู้อำนวยการหน่วยวิจัยทางคลินิก มหาวิทยาลัยอ็อกซ์ฟอร์ด ระบุว่า เวียดนามเป็นผู้นำด้านการทดลองยาต้านมาลาเรียมาตั้งแต่ปี พ.ศ. 2534 และให้ประโยชน์แก่ผู้ป่วยหลายล้านคนทั่วโลก ด้วยประชากรประมาณ 100 ล้านคน เวียดนามจึงมีกลุ่มผู้ป่วยที่หลากหลาย ซึ่งเหมาะอย่างยิ่งสำหรับการทดลองทางคลินิก อัตราการเติบโตของ GDP เฉลี่ย 6-7% ต่อปี และการเติบโตของชนชั้นกลาง ยิ่งเพิ่มความน่าดึงดูดใจของเวียดนามต่อผู้สนับสนุนทั้งในและต่างประเทศ แม้จะมีศักยภาพสูง แต่ตลาดการทดลองทางคลินิกในเวียดนามยังคงเผชิญกับอุปสรรคมากมายที่ทำให้การพัฒนาล่าช้าและไม่สอดคล้องกัน ระยะเวลาการอนุมัติการทดลองทางคลินิกในเวียดนามอาจใช้เวลานานถึง 160 วัน ซึ่งยาวนานที่สุดในเอเชีย ขณะที่ระยะเวลาเฉลี่ยสำหรับประเทศอื่นๆ อยู่ที่ประมาณ 75 วัน อันที่จริง เวียดนามยังตามหลังหลายประเทศในภูมิภาคนี้อยู่มาก เช่น สิงคโปร์ (18 วัน) อินโดนีเซีย (20 วัน) และญี่ปุ่น (31 วัน)... ช่วงเวลานี้ส่งผลต่อความน่าดึงดูดใจของตลาดเวียดนามต่อผู้สนับสนุนการวิจัย
นอกจากนี้ การทดลองทางคลินิกยังต้องอาศัยการประสานงานอย่างใกล้ชิดระหว่างแพทย์ พยาบาล ผู้ประสานงานการวิจัย และผู้จัดการข้อมูล อย่างไรก็ตาม ปัจจุบันเวียดนามยังขาดทีมงานที่ผ่านการฝึกอบรมมาเป็นอย่างดี ปัญหาทางการเงิน และกลไกจูงใจ การทดลองระยะที่ 3 อาจมีค่าใช้จ่ายตั้งแต่ 10 ถึง 20 ล้านดอลลาร์สหรัฐ ขณะเดียวกัน นักลงทุนหลายรายรายงานว่าเวียดนามขาดแรงจูงใจทางภาษี เงินทุนวิจัย หรือกลไกการร่วมทุนเช่นเดียวกับในสิงคโปร์และเกาหลีใต้ การเบิกจ่ายเงินทุนมักล่าช้าเนื่องจากขั้นตอนการบริหาร ซึ่งส่งผลกระทบต่อความคืบหน้าของการทดลองและลดความสามารถในการแข่งขันเมื่อเทียบกับประเทศอื่นๆ ในภูมิภาค
เพื่อพัฒนาอุตสาหกรรมการทดลองทางคลินิกในเวียดนาม ดร. ฟาน ตัน ทวน กล่าวว่า จำเป็นต้องลดความซับซ้อนของขั้นตอนการอนุมัติผ่านระบบออนไลน์แบบรวมศูนย์ เพื่อลดขั้นตอนอนุมัติที่ซับซ้อนในปัจจุบัน นอกจากนี้ จำเป็นต้องใช้แบบฟอร์มลงทะเบียนออนไลน์ผ่านพอร์ทัลออนไลน์ภาษาอังกฤษ และนำเอกสารสองภาษามาใช้เพื่อปรับปรุงกระบวนการสำหรับผู้สนับสนุนจากต่างประเทศ การแข่งขันกับประเทศต่างๆ ในภูมิภาคจึงจำเป็นต้องพัฒนานโยบายที่ให้สิทธิพิเศษ เช่น การยกเว้นภาษี การให้ทุนสนับสนุนการวิจัย หรือกลไกการร่วมทุนสำหรับค่าใช้จ่ายในการทดลองวิจัย เช่นเดียวกับโครงการในสิงคโปร์และไทย
“เวียดนามควรส่งเสริมรูปแบบความร่วมมือระหว่างภาครัฐและเอกชนในสาขาการวิจัยทางคลินิก เพื่อช่วยแบ่งปันความเสี่ยงและเพิ่มทรัพยากรสำหรับการพัฒนาอุตสาหกรรมอย่างยั่งยืน นอกจากนี้ จำเป็นต้องมีนโยบายการลงทุนในโครงสร้างพื้นฐาน การเพิ่มศูนย์ทดสอบ และการขยายโครงการฝึกอบรมเฉพาะทางสำหรับบุคลากร ผ่านความร่วมมือกับมหาวิทยาลัยและองค์กรระหว่างประเทศ” ดร. ฟาน ตัน ทวน เสนอ
คุณลุค เทรโลอาร์ หัวหน้าฝ่ายโครงสร้างพื้นฐาน ภาครัฐ และการดูแลสุขภาพ KPMG เวียดนาม: การสร้างนโยบายจูงใจ
กระบวนการอนุมัติการทดลองทางคลินิกในเวียดนามมีหลายขั้นตอน ขั้นตอนแรก การอนุมัติในระดับท้องถิ่นใช้เวลา 3-12 เดือน ขึ้นอยู่กับจำนวนและสถานที่ศึกษา ขั้นตอนต่อไปคือ การอนุมัติที่กระทรวงสาธารณสุขใช้เวลาประมาณ 3-5 เดือน และขั้นตอนสุดท้ายคือการยื่นขอใบอนุญาตนำเข้ายา (สำหรับการทดลองยา) ใช้เวลาเฉลี่ย 3-4 เดือน จำนวนศูนย์วิจัยและการทดลองทางคลินิกในเวียดนามยังน้อยเกินไปเมื่อเทียบกับจำนวนประชากรทั้งหมด และมีความเสี่ยงที่จะล้าหลังในการแข่งขันเพื่อก้าวขึ้นเป็นศูนย์วิจัยทางคลินิกระดับภูมิภาค เวียดนามจำเป็นต้องมีนโยบายการลงทุนด้านโครงสร้างพื้นฐาน การเพิ่มสถานที่ทดสอบ และการขยายโครงการฝึกอบรมเฉพาะทางสำหรับบุคลากรผ่านความร่วมมือกับมหาวิทยาลัยและองค์กรระหว่างประเทศ เพื่อแข่งขันกับประเทศต่างๆ ในภูมิภาค จำเป็นต้องพัฒนานโยบายที่ให้สิทธิพิเศษ เช่น การยกเว้นภาษี การให้ทุนสนับสนุนการวิจัย หรือกลไกการร่วมทุนสำหรับค่าใช้จ่ายในการทดสอบ เช่นเดียวกับโครงการในสิงคโปร์และไทย
นายเหงียน โง กวาง ผู้อำนวยการกรมวิทยาศาสตร์ เทคโนโลยี และการฝึกอบรม (กระทรวงสาธารณสุข): การกำหนดมาตรฐานกิจกรรมการทดลองทางคลินิก
ในอนาคตอันใกล้นี้ กระทรวงสาธารณสุขจะเดินหน้าปรับปรุงกรอบกฎหมาย กำหนดมาตรฐานกิจกรรมการทดลองทางคลินิกให้เป็นไปตามมาตรฐานสากล ขณะเดียวกัน เสริมสร้างศักยภาพของสภาจริยธรรมแห่งชาติด้านการวิจัยทางชีวการแพทย์ ปัจจุบันกระทรวงสาธารณสุขกำลังรับฟังความคิดเห็นเกี่ยวกับร่างหนังสือเวียนว่าด้วยกิจกรรมการทดลองยาทางคลินิก หนังสือเวียนฉบับนี้จะอธิบายรายละเอียดเกี่ยวกับกิจกรรมการทดลองยาทางคลินิก ซึ่งรวมถึงหลักการ มาตรฐาน ขั้นตอน และความรับผิดชอบที่เกี่ยวข้องกับการทดลองยาในอาสาสมัคร เพื่อประเมินความปลอดภัยและประสิทธิภาพของยา ระบุอาการไม่พึงประสงค์จากยา (ADR) และศึกษาเภสัชจลนศาสตร์ของยา ร่างหนังสือเวียนระบุว่า หลักการของการทดลองยาทางคลินิกต้องคำนึงถึงความเป็นวิทยาศาสตร์ ความเที่ยงธรรม ความซื่อสัตย์ ความโปร่งใส และการคุ้มครองสิทธิของผู้เข้าร่วมการวิจัย
MINH NAM - MINH KHA NG บันทึกแล้ว
ที่มา: https://www.sggp.org.vn/gian-nan-thu-nghiem-lam-sang-post802539.html



![[ภาพ] การประชุมครั้งแรกของคณะกรรมการความร่วมมือระหว่างสมัชชาแห่งชาติเวียดนามและสภาประชาชนแห่งชาติจีน](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2025/8/31/f5ed4def2e8f48e1a69b31464d355e12)
![[ภาพ] ประธานสภาแห่งชาติ Tran Thanh Man ต้อนรับและหารือกับประธานสภาประชาชนแห่งชาติจีน Zhao Leji](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2025/8/31/9fa5b4d3f67d450682c03d35cabba711)
![[ภาพ] ร่วมเดินขบวนในหัวใจประชาชน](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2025/8/31/8b778f9202e54a60919734e6f1d938c3)
![[ภาพ] เลขาธิการโต ลัม ต้อนรับประธานสภาประชาชนแห่งชาติจีน จ้าว เล่อจี](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2025/8/31/5af9b8d4ba2143348afe1c7ce6b7fa04)























































































การแสดงความคิดเห็น (0)